 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应H2(g) + ½O2(g) = H2O(l)△Hθ =-285.8KJ/mol则下列结论正确的是()
A.H(反应物)>H(生成物)
B.H(反应物)<H(生成物)
C.H(反应物)=H(生成物)
D.反应吸热
 答案
答案
A、H(反应物)>H(生成物)
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.H(反应物)>H(生成物)
B.H(反应物)<H(生成物)
C.H(反应物)=H(生成物)
D.反应吸热
 答案
答案
A、H(反应物)>H(生成物)
 更多“已知反应H2(g) + ½O2(g) = H2O(l)△Hθ =-285.8KJ/mol则下列结论正确的是()”相关的问题
更多“已知反应H2(g) + ½O2(g) = H2O(l)△Hθ =-285.8KJ/mol则下列结论正确的是()”相关的问题
第1题
A.K1+K2
B.K1-K2
C.K1?K2
D.K1/K2
第2题
A.热化学方程式中化学计量数表示分子数
B.该反应ΔH2大于零
C.该反应ΔH2=-571.6 kJ·mol-1
D.该反应与上述反应属于可逆反应
第3题
.已知298.15K时,反应H2(g)+
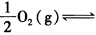 H2O(g)的△rGmΘ为一228.57kJ/mol。298.15K时水的饱和蒸汽压为3.1663kPa,水的密度为997kg/m3。求298.15K反应H2(g)+
H2O(g)的△rGmΘ为一228.57kJ/mol。298.15K时水的饱和蒸汽压为3.1663kPa,水的密度为997kg/m3。求298.15K反应H2(g)+
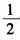 O2(g)==H2O(1)的△rGmΘ。
O2(g)==H2O(1)的△rGmΘ。
第4题
A.热化学方程式中的化学计量数表示分子数
B.该反应中的ΔH2>0
C.该反应中的ΔH2=-571.6 kJ/mol
D.该反应与题述反应互为可逆反应
第5题
A.12ΔH3+5ΔH2-2ΔH1
B.2ΔH1-5ΔH2-12ΔH3
C.12ΔH3-5ΔH2-2ΔH1
D.ΔH1-5ΔH2-12ΔH3
第6题
A.-252.9 kJ·mol-1
B.+252.9 kJ·mol-1
C.-604.5 kJ·mol-1
D.+604.5 kJ·mol-1
第7题
A.1:1
B.1:3
C.1:4
D.2:3
第8题
A.1∶1
B.1∶3
C.1∶4
D.2∶3
第9题
已知数据(298.15K)(如表5-2所示)。
表5-2 | |||||
物质 | C(石墨) | H2(g) | N2(g) | O2(g) | CO(NH2)2(s) |
S_{m}^{Theta }/(Jcdot mol^{-1}cdot K^{-1}) | 5.740 | 130.68 | 191.6 | 205.14 | 104.6 |
Delta _{c}H_{m}^{Theta }/(kJcdot mol^{-1}) | -393.51 | -285.83 | 0 | 0 | -631.66 |
物质 | NH3(g) | CO2(g) | H2O(g) |
Delta _{f}G_{m}^{Theta }/(kJcdot mol^{-1}) | -16.5 | -394.36 | -228.57 |
求:298.15K下,CO(NH2)2(s)的标准摩尔生成吉布斯函数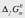 ,以及反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)的KΘ。
,以及反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)的KΘ。
第11题
A.碳的燃烧热ΔH为0.5ΔH1 kJ/mol
B.②能表示CO燃烧热的热化学方程式
C.碳的燃烧热ΔH=0.5(ΔH1+ΔH2)
D.碳的燃烧热小于CO的燃烧热